多重光散射技术快速检测液态制剂物理稳定性
多重光散射技术快速检测液态制剂物理稳定性
尹利辉 1,韩斅2
(1.中国食品药品检定研究院,北京 100050;2.北京朗迪森科技有限公司,北京 100101)
摘 要 液体制剂(liquid pharmacokinetical preparations ) 是指将药物分散在液体分散介质中,组成的内服或外用的制剂。有些液体制剂是热力学不稳定体系,随着时间的增加,会发生絮凝、上浮或沉淀等物理不稳定现象。因此,液体制剂的稳定性研究是制剂研发的关键步骤之一。本文简要介绍一种全新多重光散射(Multiple Light scattering,MLS)TURBISCAN技术,快速检测液体制剂的稳定性。该技术不需要对液体制剂有任何稀释和任何非自然力破坏,相比肉眼观察,可以节约大约200倍老化观察时间[1]。该技术解决了传统的稳定性测试方法存在的检测时间长、加速试验数据误差大等问题,并已广泛应用于食品、医药、石油、涂料、墨水等领域[2-6]。
关键词 物理稳定性; Turbiscan;多重光散射 乳液; 悬浮液药物
中图分类号 O657.39
Rapid Discrimination for Physical Stability of Liquid Pharmacokinetic Preparation by Multiple Light Scattering (MLS)
Yin Li-hui1,Han Xiao2
(1,National Institutes for Food and Drug Control, Beijing 100050,China.2, Beijing LDS Technology Limited, Beijing 100101)
Abstract Liquid pharmacokinetic preparation, which is dissolved drug in solvent, can be taken medicine orally or externally. Since some liquid pharmacokinetic preparation is a thermodynamic unstable system, the solution will have some physical instability such as creaming/sedimentation and flocculation/aggregation with the increase of time. Therefore, The stability of liquid preparation is one of the key steps in the development of the liquid pharmacokinetic preparation. This paper introduces the Multiple Light Scattering (MLS) TURBISCAN technology, which can quickly detect the stability of the solution. This technique does not require any dilution or any destruction of non nature forces of the liquid pharmacokinetic preparation; in addition, MLS TURBISCAN only takes about 1/200 of time to detect the trend of changing in the solution comparing with observation made by naked eyes [1]. The MLS TURBISCAN technology solves many problems in tradition stability detection methods, such as time consuming and large experimental error in acceleration experiment. This technique has been used in food, medicine, petroleum, paint, ink and other fields of production [2-6].
Key words The physical stability; Turbiscan;Multiple Light Scattering; Emulsion;Suspension
药物的液体制剂(liquid pharmacokinetical preparations)是指药物分散在液体分散介质中组成的内服或外用的制剂。液体制剂除具有胶囊和片剂的优点以外,还具有下列独特的优越性:1、便于口服,可以改善病人的服药顺从性,特别适合吞咽困难的病人(如儿童和老人);2、流动性好,可以根据个体对剂量需求的不同进行分剂量;3、口服后在胃肠道分布面积大,吸收彻底,生物利用程度高;4、颗粒很小,可减少对胃肠道的刺激,且体内过程受胃排空的影响小;5、可以满足将大剂量药物制成缓控释制剂的要求。[7]但是,液体制剂属多相复合体系,在热力学上属于不稳定体系,随着时间的增加,会发生絮凝、上浮或沉淀等物理不稳定现象。因此提高其稳定性,是液体制剂研发中关键步骤之一。 如何快速的评价一个液体制剂的稳定性并研究其不稳定的机理,是每一个液体制剂研发者一个迫切需要解决的问题。
Turbiscan多重光散射仪,采用经典的米氏多重光散射技术为原理,能够快速鉴定稳定性、分析失稳原因、分析粒径变化速度、粒子迁移速度、实时动态检测不稳定性等,且能够精确定量地比较样品的稳定性,分析样品不稳定机理。
Turbiscan多重光散射仪作为一项全新的实验手段和强有力的研究仪器,近年来已在诸多领域显示出其强大的优势和生命力,将分散体系稳定性研究的深度和精度大幅拓展。本文首次阐述了Turbiscan多重光散射仪测量原理以及在液体制剂(悬浮剂、乳剂、其他药剂)稳定性研究中的应用。
1、概述
1.1多重光散射原理
多重光散射是光束与液体中随机分布的多个颗粒产生相互作用的现象。入射光子在被吸收或穿透样品前,如遇到颗粒,就会散射。如果被散射的光子从样品中穿透,则形成透射光信号;如果样品浓度较高,散射光会被颗粒反射,则形成背散射光信号。多重光散射符合经典米氏理论,即不论是透射光的光强值,还是背散射光的光强值,都与光子在样品中所走过的路程(光子自由程λ*值)有关。而光子自由程λ*值,是由分散体系中颗粒的浓度和粒径决定的。因此,光强的变化,反应的是液体制剂中颗粒浓度和颗粒粒径的变化。
1.2多重光散射工作原理
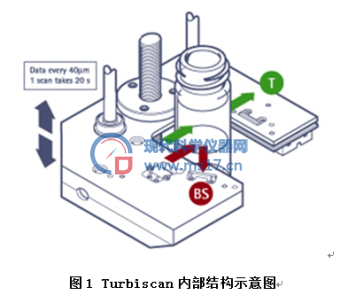
Turbiscan多重光散射仪是由一个脉冲式的近红外光源 (波长880 nm )和两个同步的检测器组成:透射光检测器是用于研究透明清澈的产品,背散射光检测器是用于研究高浓度的产品(最高浓度可达95%体积百分比)(见图1)。样品装在中央圆柱形的石英玻璃瓶中,检测探头沿着样品池高度方向,在55mm高度上进行扫描,每40微米采集一个数据点。根据设定的扫描间隔程序,不断对样品重复扫描,并收集透射光和背散射光的数据,从而得到一张表征产品稳定性特征的指纹图谱。
1.3 Turbiscan多重光散射仪技术特点
1.3.1 操作方便。Turbiscan多重光散射仪不需要任何的样品前处理工作。对高浓度的样品不需要任何稀释。检测是非浸入式的,对样品没有任何的破坏。因此测量得到的结果最为真实。
1.3.2 仪器具有极高的灵敏度。可以在分散在液体制剂的微粒发生变化的初期,扑捉到颗粒浓度和颗粒粒径变化的速度,从而推导出样品的货架期。相比肉眼观察,可以节约大约200倍的时间。
1.3.3 仪器可以给出在高浓度下,颗粒粒径变化的信息。根据这些信息,可以研究样品不稳定的机理,为配方的改进提供依据。
1.3.4能够进行定性和定量分析。
1.4多重光散射仪TURBISCAN主要功能
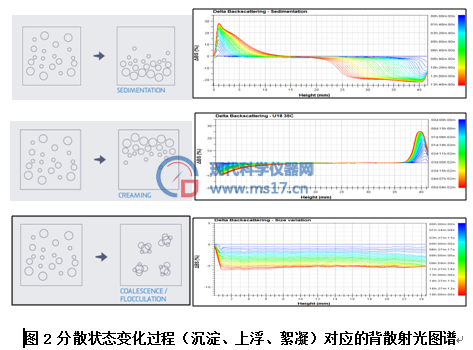
多重光散射仪TURBISCAN以光强信号做为纵坐标,样品池高度作为横坐标绘制成透射光和背散射光图谱,散射光图谱不仅能观察样品各个层面的浓度分布状态,也可定性地判断样品的粒径变化程度,持续监测样品的稳定性变化过程[8]。见图2。
例如悬浮剂药物底部的背散射光强度随时间逐渐增加,顶部光强值降低,则说明药物体系有沉淀的趋势。如果背散射光中部区域的曲线发生平行上升或下降则说明药物体系有颗粒聚集的趋势(絮凝或聚并),最终反映为粒径的变化[9,10]。在药物配方中,一些学者认为光强变化小于2%时配方是稳定的,光强度变化超过10%时就是不稳定的[11,12]。
1.4.1 实时检测定量药物中颗粒的粒径变化过程。
由于表面自由能的存在,药物颗粒在液体中会逐渐絮凝,粒径变化的快慢无疑影响着药物的最终使用性能及安全性。2009年华东理工大学的徐峰等人研究了装载血红蛋白聚合物粒子悬浮液的表面电荷调节方法,并用Turbiscan测试了表面电荷对悬浮液的稳定性影响。实验发现,未处理的悬浮液放置5d后,散射光强度的变化值为4.22%,而已调节表面电荷的悬浮液散射光强度的变化值为1.78%。这说明,表面电荷影响了样品的zeta电位最终造成了悬浮液不同的絮凝程度[13]。
1.4.2实时检测液体制剂中颗粒迁移速度
分散颗粒或液滴的形状、密度、连续相粘度均影响药剂中颗粒的迁移速度,颗粒迁移越快越容易发生沉淀和上浮现象。Turbiscan可以精确地检测药品中颗粒的迁移速度。Luis Alfonso Trujillo-Cayado等人[14]于2014年研究了两种生物友好乳液的吸附和乳化性能,测试了不同配方的背散射光图谱和上浮指数。数据表明,使用Levenol H&B作为乳化剂的配方稳定性更强,样品在一定时间后才开始出现上浮。Hideo Terayama等人[15]于2001年研究了不同表面活性剂和聚合物对药物颗粒的分散行为影响。Turbiscan沉淀速度数据显示随着纤维素加量增加,不同表面活性剂分散体系的沉淀速率越来越低,这是由于高分子吸附层的空间位阻增加引起的。另一方面,分散剂SDS和聚合物SH组成的分散体系具有最佳的稳定性,这是因为聚合物吸附了SDS,由于SDS的静电斥力产生了更高的空间位阻作用。[16]。
1.5多重光散射仪TURBISCAN目前存在的局限性
多重光散射仪TURBISCAN测量得到的光强值是经过多重散射,很多个颗粒共同作用的结果。根据多重光散射理论,不论是透射光光强值,还是背散射光的光强值,都是由体系颗粒的粒径和浓度决定的。因此计算颗粒粒径需要确切的体积浓度的信息。而且,得到的是体系体积平均粒径。 TUBISCAN LAB采用近红外光源,对小颗粒有绕过作用。因此,在测量小颗粒时,需要的浓度比较高。对于小分子药物几十纳米范围药物且浓度极稀的体系不适用。对于高浓度体系,高的浓度弥补了由于激光的绕过作用造成的灵敏度不够的缺陷。因此,该方法特别适合高浓度分散体系。弥补了经典的DLS(动态光散射)、激光粒度测定仪、多角度散射仪等相关技术不法测量高浓度样品的缺陷。
2.Turbiscan多重光散射仪在液体制剂科研领域中的应用
2.1 Turbiscan在悬浮剂药物中的应用
Turbiscan多重光散射仪在悬浮剂药物领域有广泛应用。例如监测悬浮剂药物的失稳过程:2014年Patricia G M等人[17]利用Turbiscan Lab完整测试了人类间质干细胞悬浮液的失稳过程,用于指导动脉内的严重肢体缺血的临床应用。文章表明,从背散射光曲线可以看出,人类间质干细胞悬浮液在室温条件下2h之内光强基本没有变化,比较稳定;2-6h直接背散射光信号开始整体上升,顶部出现向上的峰,证明悬浮液开始发生絮凝和上浮,最终在7h后光强不再变化,样品失稳过程完成。最终医药产品的稳定性研究表明,药物可以发生变化前送达患者体内。
悬浮药剂的制备方法与最终的稳定性也有非常大的关系,北京理工大学的药理和毒理学院的Zhenbo Yang等人[18]采用新颖的乙二醇液体复合方法制备了装载羟基喜树碱的血清蛋白纳米颗粒,并用Turbiscan快速测定了药物不同装载方法对最终悬浮剂药物的稳定性影响。实验确认了充分混合装载的悬浮剂稳定性比声波混合法和简单混合法的稳定性更好,并获得了纳米颗粒不同分散状态的SEM和TEM照片。
在判定药物稳定性方面,Turbiscan多重光散射仪也有重要的应用。E. Gonzalez-Mira等人[19]研究了配方对氟比洛芬纳米药物颗粒分散体系的综合影响,采用超声方法制备的FB-NLC12分散体系平均粒径为288nm,Turbiscan多重光散射仪在短时间内显示分散体系产生了一定程度的粒径变化,这与3个月后的LD粒径测结果一致,因为此时平均粒径已经达到亚微米级别。2012年Alexandra Hill[20]研究了不同物理参数对纳米悬浮液药物释放的过程的影响,并用Turbiscan多重光散射仪研究了纳米悬浮液的沉淀情况,实验发现纳米悬浮液底部出现一定程度的沉淀,以背散射光强度超过15%作为判断沉淀厚度的准则,确定纳米悬浮剂在3h内沉淀厚度小于1mm。2014年N. Provenza等人[21]利用Turbiscan多重光散射仪研究了西地那非儿童口服药配方的物理化学稳定性。与想象的一样,被研究的口服药配方是一个不稳定体系,样品底部出现了沉淀,中部的背散射光曲线发生了平行迁移,说明其粒径有增加的趋势。90天后的粒径测试证明了该悬浮药物配方的确发生了絮凝。这说明Turbiscan多重光散射仪可以准确预测药物是否有粒径变化的趋势,从而预测药物的长期稳定性。
2.2 Turbiscan多重光散射仪在乳剂药物中的应用
Turbiscan多重光散射仪在乳剂药物的稳定性领域也有广泛应用。药物乳剂与悬浮剂不同,因为其分散相大多为油类或脂质体,分散相的密度要小于连续相,所以乳剂的不稳定现象多以上浮为主。纳米胶囊多属于乳剂药物,例如Alfeu Zanotto-Filho、Eduardo A. Bender、Donato Cosco等人 [22][23][24]研究的纳米胶囊体系均属于乳剂体系,并使用Turbiscan多重光散射仪在短时间内测试了纳米胶囊体系的物理稳定性。
在亚微米乳液中,Turbiscan多重光散射仪也可以很好的应用,例如Miguel Wulff-Pérez等人[25]使用Turbiscan多重光散射仪测试了口服和经脉乳剂药物的稳定性,实验发现,样品池所有位置的光强没有发生改变。说明该乳剂是稳定的,同时这一结论与使用动态光散射仪测试粒径的结果相符合。
Christian Celia等人[12]制备的乳剂药物分散剂为醇质体,是一种新型经皮给药载体,也是一种特殊的脂质体。醇质体中添加了较高浓度的醇,形成渗透性和包封率更好的脂质囊泡,具有优良的稳定性和皮肤耐受性;使用Turbiscan多重光散射仪评价含有亚油酸囊泡的药物载体(如双层膜流化剂的模型)的稳定性,结果表明Turbiscan多重光散射仪可用于研究胶体制剂的稳定性。
2.3 Turbiscan多重光散射仪在其他药剂中的应用
Turbiscan多重光散射仪在高浓度或高粘度药物稳定性的研究中显示出明显的优势,而药物的物理稳定性与药物释放和应用的关系越来越密切,因此Turbiscan多重光散射仪在其他剂型药物中,也是具有重要作用。
2015年Olga Krasodomska等人[26]研发了用于肠道给药的交联壳聚糖/脂质体混合多分散体系,并用Turbiscan多重光散射仪测试了3种不同脂质体在不同温度下的稳定性情况,并用TSI进行了排序,稳定性测试结果与使用动态光散射仪的结论一致。
2012年Maria D. Moya-Ortega等人[27]综述了环糊精基础的纳米微凝胶在制药和生物领域的应用。文中表明,Turbiscan多重光散射仪可以测试用于测试纳米微凝胶的稳定性。
Ketan Sharma等人[28]制备了交联壳聚糖纳米颗粒配合定量雾化吸入器用于肺部给药。并用Turbiscan多重光散射仪研究了纳米颗粒分散体系的物理稳定性,实验发现加入PEG 600并不能完全抑制纳米颗粒的絮凝,只是将纳米颗粒的絮凝速度减缓了。这个结论说明Turbiscan多重光散射仪可以在短时间内预测药物的应用时间。
3、展望
Turbiscan多重光散射仪作为全新的实验手段和强有力的研究工具,已在诸多领域显示出强大的优势和生命力,为科研工作创造了条件。Turbiscan多重光散射仪的灵敏度和分辨率远远高于肉眼观察,检测高浓度样品无需稀释。该仪器无接触测量的检测方式,允许人们在自然环境中观测和检验样品,因此得到测量结果最为真实。随着科学研究的飞速发展,新的检测方法和技术层出不穷,单纯依靠某种技术、某种仪器远不能满足现代研究的需求,Turbiscan多重光散射仪将随着设备和应用技术的不断完善,与其它检测手段联合互补,在未来的医药科研中发挥更加重要的作用,有广阔的应用前景。
参考文献
[1]Fernández Campos, ultrastructural effects and release studies. Pharm. [J].2012.Sci. 101, 3739–3752.
[2] DonatoCosco,Aqueous-core PEG-coated PLA nanocapsules for an efficient entrapment of water soluble anticancer drugs and a smart therapeutic response;European Journal of Pharmaceutics and Biopharmaceutics [J]2015(89)30–39
[3] K. Kolter,Polyvinyl acetate-based film coatings;International Journal of Pharmaceutics [J] 2013 (457) 470– 479
[4] A.B.Jódar-Reyes,Different stability regimes of oil-in-water emulsions in the presence of bile salts;Food Research International [J]2010 (43)1634–1641
[5] Daniel Pando;Formulation of resveratrol entrapped niosomes for topical use Colloids and Surfaces B: Biointerfaces[J] 2015 (128) 398–404
[6] Chetan M. Patel; Effects of operating parameters on the production of barium sulfate nanoparticlesin stirred media mill;Journal of Industrial and Engineering Chemistry [J]2012 (18) 1450–1457
[7]王铭洲,新型液体缓控释制剂在国内的研究进展 ,畜牧与饲料科学 2012,33(2):41-43
[8]Olivier Mengual. et al, Characterisation of instability of concentrated dispersions by a new optical analyser: the TURBISCAN MA 1000. Colloids and SurfacesA: Physicochemical and Engineering Aspects [J] 1999 (152) 111–123
[9] Cristina G., Co-encapsulation of imiquimod and copaiba oil in novel nanostructured systems: promising formulations against skin carcinoma. Pharmaceutical Sciences [J] 2015 (79) 36-43
[10] Araujo, J., Nanostructured lipid carriers for triamcinolone acetonide delivery to the posterior segment of the eye. Colloids Surf. B: Biointerfaces [J] 2011 (88) 150–157.
[11] Gonzalez-Mira, E., Design and ocular tolerance of flurbiprofen loaded ultrasound-engineered NLC. Colloids Surf. B: Biointerfaces [J]2010 (81)412–421.
[12]Christian Celia, Turbiscan Lab Expert analysis of the stability of ethosomes And ultradeformable liposomes containing a bilayer fluidizing agent, Colloid Surface B[J]2009,(72 ):155-160.
[13] F. Xu et al. Long-circulation of hemoglobin-loaded polymeric nanoparticles as oxygen carriers with modulated surface charges. International Journal of Pharmaceutics[J] 2009 (377) 199–20.
[14] Patricia G M, Study of the stability of packaging and storage conditions of human mesenchymal stem cell for intra-arterial clinical application in patient with critical limb ischemia. European Journal of Pharmaceutics and Biopharmaceutics [J] 2014 (86) 459–468
[15]Hideo Terayama, Aqueous dispersion behavior of drug particles by addition of surfactant and polymer. Colloids and Surfaces B: Biointerfaces [J] 2001 (20) 73–77
[16]Fernández Campos, F., Development and characterization of a novel nystatin-loaded nanoemulsion for the buccal treatment of candidosis: ultrastructural effects and release studies. Pharm. [J].2012 (Sci. 101)3739–3752.
[17] Patricia G M, Study of the stability of packaging and storage conditions of human mesenchymal stem cell for intra-arterial clinical application in patient with critical limb ischemia. European Journal of Pharmaceutics and Biopharmaceutics [J] 2014 (86) 459–468
[18] Zhenbo Yang. et al, A novel drug-polyethylene glycol liquid compound method to prepare 10-hydroxycamptothecin loaded human serum albumin nanoparticle. International Journal of Pharmaceutics [J] 2015 (490) 412–428.
[19]E. Gonzalez-Mira. et al, Design and ocular tolerance of flurbiprofen loaded ultrasound-engineered NLC. Colloids and Surfaces B: Biointerfaces 2010 (81) 412–421
[20]Alexandra Hill. et al, Controlled delivery of nanosuspensions from osmotic pumps: Zero order and non-zero order kinetics. Journal of Controlled Release [J] 2012 (158) 403–412
[21]N. Provenza. et al, Design and physicochemical stability studies of paediatric oral formulations of sildenafil. International Journal of Pharmaceutics [J] 2014 (460) 234–239
[22]Alfeu Zanotto-Filho. et al, Curcumin-loaded lipid-core nanocapsules as a strategy to improve pharmacological efficacy of curcumin in glioma treatment. European Journal of Pharmaceutics and Biopharmaceutics [J] 2013 (83) 156–167
[23]Eduardo A. Bender, Hemocompatibility of poly(-caprolactone) lipid-core nanocapsules stabilized with polysorbate 80-lecithin and uncoated or coated with chitosan. International Journal of Pharmaceutics [J] 2012 (426) 271–279
[24]Donato Cosco, Aqueous-core PEG-coated PLA nanocapsules for an efficient entrapment of water soluble anticancer drugs and a smart therapeutic response. European Journal of Pharmaceutics and Biopharmaceutics[J] 2015 (89) 30–39
[25]Miguel Wulff-Pérez, Controlling lipolysis through steric surfactants: New insights on the controlled degradation of submicron emulsions after oral and intravenous administration. International Journal of Pharmaceutics [J] 2012 (423) 161–166.
[26]Olga Krasodomska. et al, Cross-linked chitosan/liposome hybrid system for the intestinal delivery of quercetin, Journal of Colloid and Interface Science [J] 2016 (461) 69-78
[27]Maria D, Cyclodextrin-based nanogels for pharmaceutical and biomedical applications. International Journal of Pharmaceutics [J] 2012 (428) 152–163
[28]Ketan Sharma.et al, Crosslinked chitosan nanoparticle formulations for delivery from pressurized metered dose inhalers. European Journal of Pharmaceutics and Biopharmaceutics [J] 2012 (81) 74–81

关注本网官方微信 随时订阅权威资讯