交换色谱法同时测定水中阴离子和Ca2+、Mg2+阳离子
王丹侠1 张建文1 沈俊毅1 张颖琦1 韩若冰1 徐映如1 邓子峰2
(1上海市虹口区疾病预防控制中心 上海 200082;2上海同济大学 上海 200092)
摘要 利用阴离子交换色谱法同时测定水中阴离子和Ca2+、Mg2+阳离子的含量。在Na2CO3淋洗液中加入一定量EDTA、EDTA与阳离子(Ca2+、Mg2+)螯合成为阴离子、螯合阴离子与常规阴离子同时在阴离子交换柱上被分离、电导检测器检测的方法,有效分离和检测了水中F-、BrO3-、Cl-、NO2-、Br-、NO3-、HPO42-、SO42- Ca2+、Mg2+10种离子。本方法准确、灵敏、重复性好,适用于饮用水中阴离子和Ca2+、Mg2+阳离子的同时测定。
关键词 阴离子交换色谱测定;阴离子;阳离子
中图分类号 TH833
Simultaneous Determination of Inorganic Anions and Cations(Ca2+ and Mg2+) in Water by Ion Chromatography
Wang danxia1,Zhang Jianwen1,Sheng Junyi1,Zhang Yingqi1,Han Ruobing1,Xu Yinru1,Deng Zifeng2
(1Shanghai Hongkou Centre for Disease Control and Prevention,Shanghai 200082,China;2Shanghai Tongji University,Shanghai200092)
Abstract The ion chromatography method was used for simultaneous determination of inorganic anions and cations(Ca2+ and Mg2+). Adding a certain amount of EDTA in the eluent, EDTA could form chelates with cations (Ca2+and Mg2+) which could be separated from other anion on anion-exchange columns,the separated ions were detected by conductivity detector. By the mehod, the ions(F-,BrO3-,Cl-,NO2-,Br-,NO3-,HPO42-,SO42-,Ca2+,Mg2+) in water were effectively separated and detected. The method is accurate ,high sensitivity for the detectin of anions and cations(Ca2+ and Mg2+) in drinking water.
Key words Ion chromatography; Anions ; Cations
离子色谱作为测定阴、阳离子的方法已获得广泛的应用[1],尤其是分析水样中的阴、阳离子。虽然根据速度、灵敏度、选择性、同时测定的能力、稳定性和可靠性来选择分析方法,离子色谱无疑提供了许多优点[2],然而传统的离子色谱在同一柱上是不能同时分离阳离子和阴离子的[3]。在通常情况下,阴离子和阳离子是在完全不同的色谱条件下分别分离和定量的[4],即对阴、阳离子的测定需分别使用阴、阳离子交换柱以及配以不同的淋洗液分别进行[5]。如果,在相同的色谱条件下,一次进样便能完成对阴阳离子的同时测定,就能很大地提高检测工作效率并降低分析成本[4]。因此,阴、阳离子的同时分离日益受到重视,并期待着能得到实际应用。丁明玉等用混合床离子色谱柱同时测定了水中的阴、阳离子[4];张文等用单柱阴离子排斥-阳离子交换色谱法同时测定了水中阴、阳离子[5]。本文采用在Na2CO3淋洗液中加入一定量的EDTA,EDTA与二价阳离子(Ca2 + , Mg2+)反应成为螯合阴离子(CaY2- , MgY2-),通过螯合阴离子在阴离子交换柱上与常规阴离子的同时分离,实现水中阴、阳离子的同时测定。
1 材料与方法
1.1 仪器
ICS-90离子色谱仪,配以RFC-30淋洗液发生器,ULTRA-ASRS II (4mm)阴离子抑制器,电导检测器(均为美国Dionex公司)。
1.2 试剂
碳酸钠、氢氧化钠、浓硫酸、乙二胺四乙酸二钠盐二水合物(EDTA)均为分析纯;碳酸镁、碳酸钙、其他阴离子钠盐的标准品均为优级纯;以上试剂均购自上海医药集团。
1.3 方法
1.3.1离子色谱工作条件
色谱柱:IonPac AS9-HC(250mm×4mm)分离柱,IonPacAG9-HC(50mm×4mm)保护柱;淋洗液:8.2mM Na2CO3-0.02mM EDTA溶液;流速:1mL/min;再生模式:化学抑制,30mM H2SO4作为再生液;进样量25µL。
1.3.2 标准配制
(1)阳离子(Ca2 + , Mg2+)标准储备液:用0.1M EDTA- 0.15M NaOH溶液溶解、稀释碳酸镁,配置1.00mL含镁阳离子1.000mg的标准储备液。同样的方法配置1.00mL含钙阳离子1.000mg的标准储备液。
(2)其他阴离子标准储备液:用去离子水溶解、稀释各阴离子的钠盐,配置1.00mL含各阴离子1.000mg的标准储备液。
(3)混合标准工作系列溶液:用去离子水稀释配置成各离子浓度范围合适的混合标准工作系列溶液(参照表1)。
1.3.3 测定
标准系列和水样分别经0.20μm的过滤膜处理后进样(进样量25μL)。以保留时间定性、峰面积定量测定水中钙、镁阳离子和其他阴离子的浓度。
计算公式:ρ=c×f
ρ:水中钙、镁阳离子和其他阴离子的浓度,mg/L;
c:被测样液中钙、镁阳离子和其他阴离子的浓度, mg/L;
f:稀释倍数。
2 结果与讨论
2.1 色谱条件的选择
2.1.1 流动相优化
(1)流动相中Na2CO3浓度的优化
为同时分离钙、镁离子及各无机阴离子,对流动相中碳酸钠浓度影响保留时间进行了研究。选用阴离子色谱柱IonPac AS9HC,配以在不同浓度水平的Na2CO3中加入一定浓度的 EDTA(EDTA浓度恒定在0.02mM),同时固定1mL/min的流速,考察混合标准的分离情况,结果见图1。图1表明,logk(k为相对保留因子)与log(CCO32-)呈线性关系;CCO32-增加时k下降、且二价离子的k下降得更快;二价阳离子(Ca2+、 Mg2+)线性斜率同二价阴离子(SO42-,HPO42-)、且二倍于单价的阴离子。据此研究,当流动相中Na2CO3为低浓度(4 mM、6 mM)时,阴、阳离子的长保留时间并没有改善它们之间的分离;当流动相中Na2CO3为高浓度(12 mM、14 mM)时,阴、阳离子之间的分离不佳,尽管它们的保留时间较短;当流动相中Na2CO3为中浓度(8 mM、10 mM)时,阴、阳离子在合适的洗脱时间里得到了良好的分离。据此作进一步研究,选8.2mM为流动相中碳酸钠的最佳浓度。

图1 淋洗液碳酸钠浓度与各离子相对保留因子之间的关系:
1.SO42-,2.HPO42-,3.NO3-,4.Br-,5.MgY2-,6. NO2-,7.CaY2-,8.Cl-
(2)流动相中EDTA浓度的优化
恒定流动相中Na2CO3浓度为8.2 mM,变化流动相中EDTA浓度如下4水平:0、0.02、0.05和0.1 mM。当流动相中EDTA浓度为0时, MgY2-峰降解。当流动项中EDTA浓度为0.02 mM时,CaY2-、MgY2-峰形对称峰宽较窄,各分析物之间的分离好。流动相中的EDTA浓度比较高为0.05 mM、0.1 mM时,柱很快就平衡了,分析物的保留时间和分辨率急剧下降,尤其是二价阴离子。另外当流动相中的EDTA浓度为0.1 mM,显著增加的电导背景降低了检测灵敏度。据此研究,选择流动相中EDTA浓度为0.02 mM。
(3)流动相中pH的优化
流动相(8.2 mM Na2CO3+0.02 mMEDTA)的pH为10.4,当通过加酸调节流动相的pH为9.5时,CaY2-、 MgY2-峰形变宽,尤其是MgY2-非常明显。这是由于pH下降使得CaY2-、MgY2-的稳定性下降,尤其对MgY2-稳定性影响更大。pH下降对其他无机阴离子峰宽没有影响。当通过加氢氧化钠调节流动相的pH为11.5时, MgY2-峰消失。据此研究,选流动相pH为10.4。
综上,经优化的流动相为:8.2 mM Na2CO3+0.02 mMEDTA, pH=10.4。
2.1.2 抑制器的选择
分析研究两种类型的抑制器:树脂填充型抑制器和平板微膜型抑制器。采用树脂填充型抑制器进行实验时,钙、镁螯合物的色谱峰有严重的拖尾情况且灵敏度、分离度都很差。但采用平板微膜抑制器则不存在此类情况,具有峰形对称、灵敏度高、分离度好等优点(见图2)。其原因是这两种抑制原理不同。树脂填充型抑制器填充的为中高交联度的常规磺酸型阳离子交换树脂,当CaY2-、MgY2-经过抑制器,pH降低接近于中性的情况下,CaY2-、MgY2-的稳定性降低,钙镁就被暂时吸附在阳离子树脂上,而这部分钙镁需要后面流动相中的EDTA才能被重新螯合洗脱出来。因此CaY2-、MgY2-洗脱被多种机理控制,形成了拖尾的情况,影响色谱行为[6]。
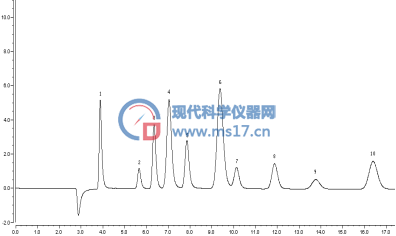
图2 标准样品色谱图
1.F-(3μg/mL)、2. BrO3-(5μg/mL)、3.Cl-(4μg/mL)、4. CaY2-(5μg/mL)、5.NO2-(6μg/mL)、
6. MgY2-(5μg/mL)、7.Br-(5μg/mL)、8.NO3-(5μg/mL)、9.HPO42-(5μg/mL)、10.SO42-(5μg/mL)
2.2 标准样品中的EDTA浓度
为评估标准系列中EDTA浓度对各离子色谱分离行为的影响,测定了含不同EDTA浓度的标准系列。当标准溶液中的EDTA浓度高于10mM时,CaY2-、MgY2-的保留时间随浓度增加而发生变化。当标准溶液中的EDTA浓度低于10mM时,CaY2-、MgY2-标准峰保留时间即便在其浓度很高(80.0μg/mL)时也保持不变。
2.3 线性范围、精密度和检出限
在选定的色谱条件下,对含有2种阳离子(Ca2 + , Mg2+)和8种阴离子(F-、BrO3-、.Cl-、.NO2-、.Br-、NO3-、.HPO42-、SO42-)的混合标准溶液进行测定,考察方法的线性范围、精密度和检出限等分析特性,结果见表1。
表1 分析方法特性
|
被测离子 |
保留时间 (min) |
半峰宽 (min) |
线性范围 (mg/L) |
回归方程 |
相关系数 (r) |
RSD峰面积 (%,n=6) |
检出限 (mg/L,S/N=3) |
|
F- |
3.88 |
0.15 |
0.10~20.0 |
y =0.4383x - 0.0072 |
0.9997 |
0.2~1 |
0.01 |
|
BrO3- |
5.56 |
0.15 |
0.10~20.0 |
y =0.0627x - 0.0053 |
0.9996 |
0.3~3 |
0.04 |
|
Cl- |
6.50 |
0.18 |
0.10~50.0 |
y =0.2812x - 0.0081 |
0.9993 |
0.2~2 |
0.02 |
|
CaY2- |
7.00 |
0.21 |
0.10~50.0 |
y =0.3890x + 0.0061 |
0.9997 |
1~2 |
0.02 |
|
NO2- |
7.81 |
0.20 |
0.10~20.0 |
y =0.1606x - 0.0034 |
0.9998 |
0.3~2 |
0.02 |
|
MgY2- |
9.50 |
0.30 |
0.10~50.0 |
y =0.4397x + 0.0256 |
0.9998 |
0.5~1 |
0.01 |
|
Br- |
10.12 |
0.20 |
0.10~20.0 |
y =0.0752x - 0.0070 |
0.9993 |
0.2~2 |
0.03 |
|
NO3- |
11.80 |
0.24 |
0.10~50.0 |
y =0.1205x - 0.0063 |
0.9993 |
0.2~2 |
0.03 |
|
HPO42- |
13.75 |
0.30 |
0.10~20.0 |
y =0.0253x - 0.0050 |
0.9998 |
0.4~3 |
0.04 |
|
SO42- |
16.50 |
0.39 |
0.10~50.0 |
y =0.2274x - 0.0055 |
0.9993 |
0.1~1 |
0.02 |
2.3.1 线性范围
二个EDTA络合物(CaY2-、MgY2-)在0-50mg/L(以金属计)浓度范围内有非常好的线性,阴离子Cl-、NO3-、SO42-的线性范围为0-50 mg/L,阴离子F-、BrO3-、NO2-、Br-、HPO42-的线性范围为0-20mg/L。
2.3.2 精密度
对高、低2种浓度(1mg/L、20mg/L)的混合标准作再现性实验(n均为6),计算以峰面积计的RSD,同其他的阴离子一样,高浓度水平Ca2+、Mg2+的RSD(1%、0.5%)低于低水平浓度的RSD(2%、1%),均小于5%,Ca2+、Mg2+同其他的阴离子一样具有良好的再现性。
2.3.3 检出限
以3倍信噪比作为检出限(25µL进样量),Ca2+和Mg2+的检出限分别为0.02mg/L和0.01mg/L,其他阴离子的检出限在0.01mg/L—0.04mg/L之间,Ca2+、Mg2+的检测能力同其他阴离子。另外,半峰宽(除CaY2-、MgY2-)随着保留时间的增加而增加,CaY2-、MgY2-半峰宽较相邻的阴离子要宽。
2.4 准确度试验
采用加标回收法测定准确度。在一水样中加入阴阳离子混合标准溶液,测定各离子加入量,计算其加标回收率。根据表2,回收率试验结果范围为95%~103%,表明本法具有满意的准确度。
表2 各离子回收率试验结果
|
被测离子 |
F- |
BrO3- |
Cl- |
CaY2- |
NO2- |
MgY2- |
Br- |
NO3- |
HPO42- |
SO42- |
|
加入量(mg/L) |
3.00 |
5.00 |
4.00 |
5.00 |
6.00 |
5.00 |
5.00 |
5.00 |
5.00 |
5.00 |
|
*实测值(mg/L, n=6) |
2.85 |
4.80 |
4.08 |
5.05 |
6.00 |
5.10 |
4.93 |
5.17 |
4.95 |
4.88 |
|
回收率(%) |
95.0 |
96.0 |
102 |
101 |
100 |
102 |
98.6 |
103 |
99.0 |
97.6 |
|
注:实测值为加标样品扣除本底后的测定值。 |
||||||||||
2.5 样品前处理
比较评估二种样品前处理方法(在水样中预先加入或不加EDTA)的离子色谱测定结果。水样直接测定的分离结果同水样预先与10mM EDTA(pH=10)混合后测定的分离情况:钙镁阳离子间、无机阴离子间及阴阳离子间的分离均良好,即使是较为相近的Cl-和Ca2+;二种前处理方法测得的钙、镁阳离子及其他阴离子的浓度值一致。故实际样品测定前不必处理,直接测定即可。
2.6 样品分析
利用该法对各类饮用水进行分析,分析结果见表3。对于本法中阴离子的测定,《生活饮用水检验方法》GB/T 8750-2006[7]中已有离子色谱测定法。对于钙、镁阳离子,国标方法是火焰原子吸收光谱法和滴定法(《饮用天然矿泉水检验方法》GB/T 8538-2008[8]),为进一步证明本研究方法的适宜性,用本法和原子吸收测定法二法测定各类饮用水中的钙、镁离子,比较二法测定的结果,分析结果见表3。两种方法测得的结果经统计计算:|t|钙=0.13
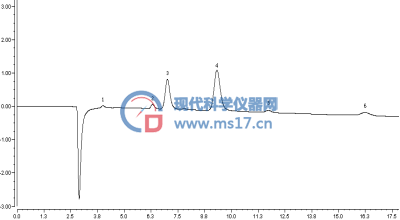
图3 样品分离色谱图
1.F-、2.Cl-、3 CaY2-、4. MgY2-、5.NO3-、6.SO42-
表3 样品分析结果
|
样品 |
质 量 浓 度(mg/L) |
||||||||||||||
|
F- |
BrO3- |
Cl- |
Ca2+ |
NO2- |
Mg2+ |
Br- |
NO3- |
HPO42- |
SO42- |
||||||
|
IC |
AAS |
IC |
AAS |
||||||||||||
|
饮用水1 |
0.1 |
n |
7.0 |
75.0 |
75.0 |
1.5 |
28.5 |
25.5 |
n |
3.9 |
n |
12.8 |
|||
|
饮用水2 |
0.1 |
n |
18.9 |
60.8 |
59.2 |
0.5 |
13.0 |
12.4 |
n |
1.5 |
n |
n |
|||
|
饮用水3 |
n |
n |
0.37 |
53.8 |
55.2 |
n |
11.5 |
10.9 |
n |
n |
n |
0.73 |
|||
|
饮用水4 |
n |
n |
3.98 |
41.9 |
42.8 |
0.6 |
10.3 |
9.3 |
n |
1.5 |
n |
5.30 |
|||
|
饮用水5 |
n |
n |
2.43 |
41.5 |
41.5 |
n |
10.5 |
9.5 |
n |
n |
n |
n |
|||
|
饮用水6 |
n |
n |
2.29 |
33.6 |
34.5 |
n |
8.4 |
7.4 |
n |
n |
n |
n |
|||
|
注:n表示未检出目标峰。 |
|||||||||||||||
3 结论
采用在Na2CO3淋洗液中加入一定量EDTA、EDTA与阳离子(Ca2+、Mg2+)螯合成为阴离子、螯合阴离子与常规阴离子同时在阴离子交换柱上被分离、电导检测器测定的方法,有效分离、检测了水中F-、BrO3-、Cl-、NO2-、Br-、NO3-、HPO42-、SO42-、Ca2+、Mg2+10种离子。该方法就饮用水的常规分析而言,因直接进样而无需样品的前处理使得操作简便;因阴阳离子的同时检测减少了分析时间、降低了分析成本;因较高的灵敏度以及良好的线性与重复性且没有来自其它物质的干扰等能很好地满足饮用水中上述10种阴阳离子的同时测定,同时离子色谱又是实验室常规的分析仪器。综上,本研究方法具有很好的推广应用价值。
参考文献
[1] 牟世芬,刘开录.离子色谱[M].北京:科学出版社,1986.227-258
[2] B. Lopez-Ruiz, J. Chromatogr. A 881(2000)607
[3] P.V. Nesterenko,Trends Anal.Chem.20(6-7)(2001)311
[4] 丁明玉,王宗花,陈培榕.用混合床离子色谱柱同时测定阴阳离子[J].分析化学,1997,25(12):1430-1433
[5] 张文,许群,鲜跃仲等.同时测定水中阴、阳离子的单柱阴离子排斥-阳离子交换色谱法[J].分析测试学报,2000,19(3):34-36
[6] 王丹侠,徐以盛. 工作场所空气中碳酸镁离子色谱分析方法的研究[J].现代科学仪器,2006,3:85-87
[7] GB/T 8750-2006生活饮用水检验方法[S].
[8] GB/T 8538-2008饮用天然矿泉水检验方法[S].

关注本网官方微信 随时订阅权威资讯

