过硫酸铵消化-柱前衍生-气相色谱法分析尿样中总碘和有机碘
过硫酸铵消化-柱前衍生-气相色谱法分析尿样中总碘和有机碘
叶海朋1 江阳1 周凯1 张宜明2 张力群2
(1杭州市上城区疾病预防控制中心 杭州 310009;2杭州市疾病预防控制中心 杭州 310021)
摘要 目的:建立尿总碘和有机碘的气相色谱分析方法。方法:尿样经过硫酸铵消化,无机碘和有机碘被氧化为碘酸根,再经过2-丁酮衍生化,以正己烷萃取,离心后,吸取有机层进样,经HP-5气相色谱柱分离,电子捕获检测器检测,峰面积定量。结果:该法分离效果好,检出限为0.50μg/L,加标回收率为98.2%-101.0%,相对标准偏差为1.7%-2.8%,并以差值法计算尿有机碘含量为4.1%-12.6%。结论:该方法准确简便,灵敏度高,可用于尿样中总碘和有机碘的分析测定。
关键词 消化;尿;总碘;有机碘
中图分类号 TH833
Determination of Total Iodine and Organo-iodine in Urine by Ammonium Persulfate Digestion and Gas Chromatography
Ye Haipeng1,Jiang Yang1,Zhou Kai1,Zhang Yiming2,Zhang Liqun2
(1Shangcheng District Center for Disease Control and Prevention,Hangzhou 310009,China;2Center for Disease Control and Prevention,Hangzhou 310021,China)
Abstract Objective: A gas chromatography method for the determination of total iodine and organo-iodine in urine is developed. Methods: Ammonium persulfate digestion was adopted as urine pre-treatment, which finally converted all the iodine species into iodate and derivatived with 2-butanone,then extracted by hexane. The analyte was separated on HP-5 capillary column and detected by electron capture detector(ECD), quantified by peak areas. Results: Separation of the method was good and the detection limit was 0.50μg/L with the recovery rate of 98.2% -101.0% and the relative standard deviation( RSD) was from 1.7% to 2.8%,and calculated organo-iodine content of 4.1%-12.6% in urine. Conclusion: This method is simple, sensitive and accurate. It is reliable to determine the total iodine and organo-iodine in urine.
Key words Digestion; Urine; Total Iodine; Organo-iodine
尿碘的浓度可反应机体内碘的水平,是用来评价人体营养状况的一个重要指标[1]。尿中碘含量非常低,研究表明,尿中除了以I-形式存在无机碘,还有多种存在形式的有机碘[2.3]。尿中碘总量测定,除了砷铈催化动力学分光光度法[4],研究较多的还有电感耦合等离子体质谱法[5],离子色谱串联电感耦合等离子体质谱法[6],超高效液相色谱串联电喷雾质谱法[7]。本文在国家标准尿碘和水中碘化物测定方法基础上[8],尿样经过硫酸铵消化,再进行衍生化,用毛细管柱分离,气相色谱ECD检测,建立尿中总碘的测定方法;采用差值法计算尿样中有机碘含量。与尿碘国标检测方法相比,本方法操作简便、灵敏度及准确度高,可以批量处理样品,最低检出限、相对标准偏差、稳定性等试验结果均较为理想。
1 材料与方法
1.1 仪器
6890A气相色谱仪(带μECD检测器)(美国Agilent公司);Milli-Q超纯水系统(美国Millipore公司);HP-5毛细管色谱柱(Agilent,30m×0.32mm×0.25μm),DB-1701毛细管色谱柱(Agilent,30m×0.25μm× 0.25μm);KIA-MS3旋涡混合器(德国);TDL-40B台式离心机(上海安亭科学仪器厂);自控恒温尿碘消解仪(北京博瑞赛科技有限责任公司设备公司)。
1.2 试剂
实验室自备超纯水;过硫酸铵2.0mol/L(分析纯);硫代硫酸钠2.0g/L(分析纯),现配;重铬酸钾1.0g/L(分析纯),现配;丁酮(色谱纯);环己烷(色谱纯);正己烷(色谱纯);石油醚(分析纯);甲苯(色谱纯);苯(色谱纯)。
1.3 方法原理
过硫酸铵受热分解产生活性氧,消解尿样中的有机物,同时将所有形态的碘氧化为IO3-。酸性条件下,用硫代硫酸钠将消化液中IO3-还原成I-,再被重铬酸钾氧化成单质I2。在H+条件,2-丁酮以烯醇式存在,与I2衍生化主要生成3-碘-2-丁酮再用正己烷萃取后经毛细管色谱柱分离,气相色谱仪(电子捕获检测器)检测。
1.4 色谱条件
柱温80℃保持8min,柱流量2.0mL/min;进样口温度220℃;不分流进样;检测器温度;250℃;进样量1.0μL。
1.5 标准溶液的配制
称取预先在110℃条件下烘干至恒重的碘化钾0.1308g于1L棕色容量瓶中,用纯水溶解并定容刻度,得到碘化物质量浓度为100mg/L(以I- 计)标准溶液。再用纯水逐级稀释配置浓度为0μg/L、25μg/L、50μg/L、100μg/L、300μg/L、500μg/L、800μg/L、1000μg/L(以I-计),与样品在相同条件下进行前处理并测定,取1.0μL进样,绘制标准曲线。
1.6 尿样处理与测定
取1.0mL尿样于10mL小试管中,加过硫酸铵1mL,置于尿碘消解仪,100℃消解,1小时后取出,放置冷却至室温。处理好的样品,加硫代硫酸钠0.2mL,丁酮0.2mL,混匀,放置5min,加入重铬酸钾0.2mL,混匀,放置40min,再加入苯1.0mL,旋涡混合萃取1min,以4000r/min离心5min,取上清液,经无水硫酸钠干燥后,供色谱测定。
2 结果与讨论
2.1 衍生化产物的确认分析
在H+条件,2-丁酮以烯醇式存在,与碘衍生化生成3-碘-2-丁酮和1-碘-2-丁酮,2个同分异构体保留时间和响应值存在差异,以弱极性色谱柱(HP-5)和中等极性色谱柱(DB-1701)进行双毛细管柱定性分析,如图1 所示。结果显示,主要衍生化产物3-碘-2-丁酮在HP-5色谱柱中的保留时间为3.081min,在DB-1701色谱柱中的保留时间为5.400min,两者分离度均较好,目标物无溶剂和杂质峰干扰。两者相比较,HP-5分离时间更短,适用于样品的批量检测。
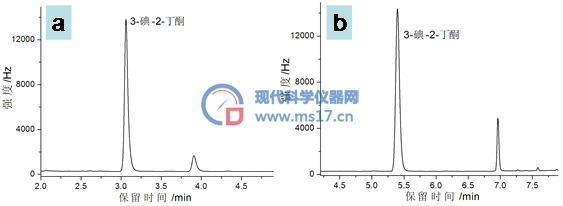
图1 双柱定性分离标准色谱图(a.HP-5色谱柱;b.DB-1701色谱柱)
Fig.1 The gas chromatogram of quantified by double capillary columns
2.2 标准曲线及方法检出限
碘离子浓度在25μg/L-1000μg/L范围内呈线性关系,直线回归方程为Y=54.76X-200.99,回归系数r=09997,线性良好,可满足定量分析的要求,按仪器的3倍噪音值计算其最低检出浓度为0.50μg/L。
2.3 样品衍生条件的选择
过硫酸铵受热分解如下所示,其产生的H+可以保持溶液一定的酸性条件,因此衍生化反应不需要额外加酸。
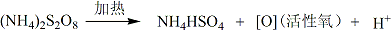
取1000μg/L标准溶液进行消化处理,加入过量的硫代硫酸钠还原碘酸根和残留的活性氧,分别取硫代硫酸钠浓度为0.5、1.0、1.5、2.0、4.0、5.0g/L进行实验比较,结果如图2所示。硫代硫酸钠浓度增加至2.0g/L时,检测到碘的浓度最大,而随着硫代硫酸钠浓度继续增加,被检测到的碘浓度呈减小趋势。
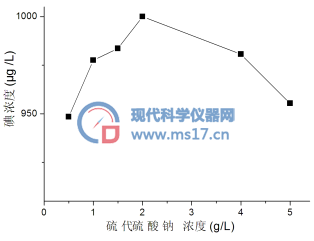
图2 硫代硫酸钠浓度对衍生化效率的影响
Fig.2 Effects of sodium thiosulfate concentration on the derivation
重铬酸钾氧化碘离子为分子碘需要一定的反应时间,试验中加入重铬酸钾溶液后分别反应10、20、30、40、60min,按本法实验,结果如图3所示。20min以内碘代丁酮的浓度明显增加,至30min时浓度最大,之后无明显变化,据此反应时间定为30min。
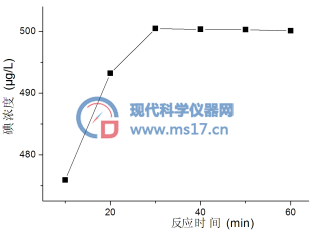
图3 反应时间对衍生化效率的影响
Fig.3 Effects of reaction time on the derivation
2.4 萃取溶剂的选择
取同一个尿样,加入碘标准使用液使其浓度为500μg/L,经消化-衍生化后分别用甲苯、苯、环己烷、正己烷、石油醚萃取,平行3次试验,计算其萃取效率,结果如图4所示。
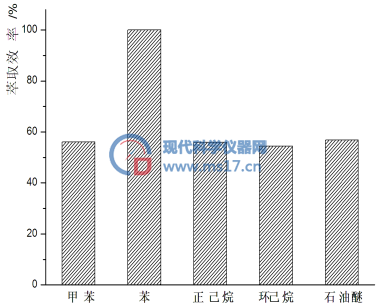
图4 不同萃取剂对碘代丁酮的萃取效率
Fig.4 The extraction efficiency of different extractants on iodine ketone derivatives
由图4可以看出,用苯萃取效率最高,其他4种溶剂萃取效率相差不大,但是苯的精制复杂,而且毒性大,使用时对检验人员的伤害很大,由于苯有非常好的溶解性,样品中的干扰物质也大量被萃取出来,在HP-5色谱柱上会干扰被测物的出峰,实际工作中选正己烷作为萃取溶剂可以满足使用要求。
2.5 方法的准确度和精密度实验
取一份健康成人尿为待测尿样,按照本方法进行消化、衍生化后利用色谱测定,以保留时间定性,峰面积定量,测得本底值。同时在尿样中分别加入高、中、低三个浓度梯度的碘,做回收率试验和精密度试验,测定结果见表1。从表1可见,其平均加标回收率为98.2%-101.0%,相对标准偏差为1.7%-2.8%,能够满足实际检测要求。
表1 方法加标回收率和精密度(n=6)实验结果
Tab.1 The standard added recoveries and relative standard deviations(n=6)
|
本底浓度(µg/L) |
加标浓度(µg/L) |
测得浓度(µg/L) |
平均浓度(µg/L) |
平均回收率(%) |
RSD (%) |
|||||
|
20.3 |
50.0 |
69.2 |
68.0 |
73.5 |
72.3 |
71.4 |
70.6 |
70.5 |
101.0 |
2.6 |
|
20.3 |
200.0 |
216.3 |
210.6 |
219.4 |
225.2 |
221.1 |
207.8 |
207.8 |
98.2 |
2.8 |
|
20.3 |
500.0 |
511.2 |
504.2 |
525.4 |
505.4 |
513.2 |
527.0 |
514.4 |
98.8 |
1.7 |
2.6 尿样稳定性试验
选择2.5制备的加标尿样,按照WS/T107-2006尿样的保存方法,置于4℃的冰箱中,于放置当天和2个月取样测定含量,每次测定平行样品6次,试验结果见表2。表2可以看出,各浓度样品在4℃保存2月后,其下降率均<10%,而且保存放置对高浓度样品影响比低浓度影响小。
表2 样品稳定性试验
Tab.2 The test of sample stability
|
尿样 |
保存时间 |
测得浓度(µg/L) |
平均浓度(µg/L) |
下降率(%) |
|||||
|
本底 |
当天 |
21.2 |
20.2 |
19.9 |
20.1 |
20.0 |
20.2 |
20.3 |
7.9 |
|
2个月 |
19.0 |
19.5 |
17.9 |
18.7 |
19.2 |
17.9 |
18.7 |
||
|
50.0µg/L |
当天 |
69.2 |
68.0 |
73.5 |
72.3 |
71.4 |
70.6 |
70.5 |
4.3 |
|
2个月 |
65.8 |
68.9 |
67.9 |
69.2 |
67.2 |
66.0 |
67.5 |
||
|
200.0µg/L |
当天 |
216.3 |
210.6 |
219.4 |
225.2 |
221.1 |
207.8 |
207.8 |
1.1 |
|
2个月 |
207.1 |
200.9 |
206.5 |
203.3 |
208.0 |
207.5 |
205.5 |
||
|
500.0µg/L |
当天 |
511.2 |
504.2 |
525.4 |
505.4 |
513.2 |
527.0 |
514.4 |
1.1 |
|
2个月 |
502.7 |
503.9 |
513.7 |
512.1 |
514.4 |
506.6 |
508.9 |
||
2.7 实际样品测定
分别取10份健康成人尿样,分别采用消化-衍生化-GC-μECD测尿总碘和直接衍生化-气相色谱法测尿中无机碘,并以差值法计算有机碘含量,结果如表3所示。结果表明,10份尿样有机碘含量为4.1%-12.6%,这与文献[2-3]研究的结果也是吻合的。
表3 尿碘形态测定结果
Tab.3 The results of iodine species test
|
碘形态 |
编号 |
|||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
|
总碘 |
51.3 |
208.9 |
84.3 |
79.7 |
176.5 |
83.2 |
97.5 |
1124.6 |
159.0 |
41.2 |
|
无机碘 |
45.4 |
186.4 |
80.1 |
76.4 |
161.1 |
78.9 |
92.8 |
983.2 |
143.0 |
39.5 |
|
有机碘 |
5.9 |
22.5 |
4.2 |
3.3 |
15.4 |
4.3 |
4.7 |
141.4 |
16.0 |
1.7 |
3 小结
本文建立的过硫酸铵消化-柱前衍生-气相色谱法测定尿总碘含量,采用差值法计算尿中有机碘含量,具有操作准确、可靠、灵敏度高的特点,可以应用于尿碘的测定及其形态分析。
参考文献
[1] 陈学敏.环境卫生学[M].第4版.北京:人民卫生出版社,2001:151
[2] Tingting Gong,Xiangru Zhang,Determination of iodide,iodate and organo-iodine in waters with a new total organic iodine measurement approach[J].Water research 47(2013),6660-6669
[3] 刘德晔,谷静,刘华良.离子色谱-电感耦合等离子体质谱联用研究尿中碘和钼形态[J].分析试验室,2013,32.7,40-44
[4] WS /T107- 2006 ,尿中碘的砷铈催化分光光度测定方法[S]
[5] P.Macours,J.C.Aubry,B.Hauquier,J.M.Boeynaems,S.Goldman,R.Moreno-Reyes,Determination of urinary iodine by inductively coupled plasma mass spectrometry[J].Journal of Trace Elements in Medicine and Biology 22 (2008) 162-165
[6] Weina Zhang,Xiaoqiu Liu,Xiaoyu Jia,et al.Fast Speciation of Iodide and Iodate in Edible Salts and Human Urine by Short Column IC Coupled with Inductively Coupled Plasma MS [J].Chromatographia 2010,72,1009-1012
[7] Yang Pan,Xiangru Zhang,Total organic iodine measurement: A new approach with UPLC/ESI-MS for off-line iodide separation/detection[J].Water research 47 (2013) 163-172
[8] GB /T5750.8-2006.生活饮用水标准检验方法有机物指标[S].

关注本网官方微信 随时订阅权威资讯

